Rutherfordovo raspršenje
Rutherfordovo raspršenje je pojava iz nuklearne fizike, kojom se objašnjava skretanja alfa-čestica koje udaraju u tanke listiće metala, a s njim se dokazuje postojanje pozitivno nabijene atomske jezgre, koja ima gotovo svu masu atoma. Rutherfordovo raspršenje je objašnjenje strukture atomske jezgre, koje je nastalo nakon pokusa s alfa-česticama i zlatnim listićem, kojeg su izveli Ernest Rutherford, Hans Geiger i Ernest Marsden. Rezultati tog pokusa su pokazali da su skretanja alfa-čestica pod velikim kutevima bila jako rijetka, na primjer pri prolazu kroz listić platine na svakih 8000 jedna alfa-čestica bi skrenula pod kutom većim od 90º.[1]


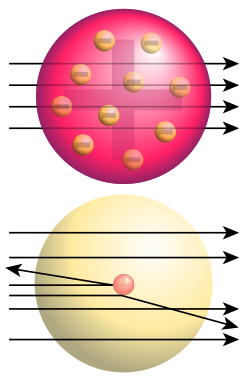
Donja slika: Dobiveni rezultati: samo mali dio alfa-čestice skreće, pokazujući da postoji pozitivan naboj u atomskoj jezgri (treba napomenuti da mjere nisu stvarne, atomska jezgra je još puno manja). To je Rutherfordov model atoma.
Matematičko objašnjenje uredi
Pokus s alfa-česticama i zlatnim listićem je bio jedan od najznačajnih pokusa u nuklearnoj fizici, jer je to bio prvi dokaz da u atomu postoji atomska jezgra. Na osnovu rezultata mnogobrojnih pokusa, s više različitih metalnih listića, Rutherford i njegovi suradnici su zaključili da pri prolazu kroz kroz metalne listiće nastaje raspršenje ili skretanje alfa-čestica. Ovu pojavu su objašnjavali međusobnim djelovanjem alfa-čestica i jezgre atoma metala, kroz koje su one prolazile.
Rutherford je pretpostavio da do skretanja dolazi zbog djelovanja Coulombove sile ili odbijajuće elektrostatičke sile između alfa-čestica s električnim nabojem Z1 i jezgre atoma s električnim nabojem Z2 (Z – atomski broj). Pošto je masa atomske jezgre metala puno veća od mase alfa-čestice, pretpostavka je da je atomska jezgra metala nepokretna. Osim toga, pretpostavka je da elektron ne utječe na skretanje alfa-čestice zbog svoje male mase.
Parametar sudara uredi
Parametar sudara b je normalna ili okomita (najkraća) udaljenost od centra električno nabijene atomske jezgre do pravca početnog kretanja električno nabijene čestice projektila. Prema Coulombovom zakonu ove dvije čestice s istim nabojem se odbijaju. Odnos između parametra sudara b i kuta skretanja θ iznosi:
gdje je: - brzina čestice projektila kada je daleko od centra atomske jezgre i rmin – najkraća udaljenost između centara dviju čestica.
Korištenjem Binetove formule jednadžba putanje alfa-čestice se može opisati:
gdje je: , – brzina čestice projektila kada je daleko od centra atomske jezgre, b – parameter sudara. Rješenje ove diferencijalne jednadžbe je:
za granične uvjete:
Vrijedi isto:
Kut skretanja Θ se može riješiti za kao:
Parametar sudara b na kraju iznosi:
Računanje veličine atomske jezgre uredi
Kod sudara alfa-čestice i atomske jezgre, sva kinetička energija alfa-čestice se pretvara u potencijalnu energiju (Coulombova sila). Zato vrijedi:
Ili nakon sređivanja:
Za alfa-čestice i zlato vrijedi::
- m (masa) = 6,7×10−27 kg
- q1 = 2×(1,6×10−19) C
- q2 (za zlato) = 79×(1,6×10−19) C
- v (početna brzina alfa-čestice) = 2×107 m/s
Računanjem dobijemo vrijednost oko 2,7×10−14 m (stvarna vrijednost polumjera atomske jezgre zlata je 7,3×10−15 m). Razlika nastaje jer alfa-čestica nema dovoljno energije da dođe toliko blizu atomske jezgre zlata. Pokusi su pokazali da se formule Rutherfordovog raspršenja slažu s rezultatima proračuna, što je dokazalo postojanje atomske jezgre. To je bio uvod u novi Rutherfordov model atoma i dokaz da se Thompsonov model atoma ne slaže s rezultatima pokusa, a time i sa stvarnošću.[2]
Izvori uredi
- ↑ E. Rutherford: "The Scattering of α and β Particles by Matter and the Structure of the Atom", Philos. Mag., 1911.
- ↑ [1][neaktivna poveznica] "Uvod u nuklearnu energetiku", Prof. dr. sc. Danilo Feretić, 2011.