Johann Wolfgang Döbereiner
Johann Wolfgang Döbereiner (Hof, 13. prosinca 1780. – Jena, 24. ožujka 1849.), njemački kemičar. Istraživanjem katalitičkih svojstava platine pridonio razvoju katalize. Svrstavši kemijske elemente sličnih svojstava u takozvane trijade (na primjer kalcij, stroncij, barij; ili sumpor, selenij, telurij), pokazao da je srednja vrijednost relativnih atomskih masa najlakšeg i najtežeg kemijskog elementa približno jednaka masi srednjeg elementa, čime je prethodio otkriću periodnoga sustava elemenata.[1]
| Johann Wolfgang Döbereiner | |
 | |
| Rođenje | 13. prosinca 1780. Hof, Bavarska, Njemačka |
|---|---|
| Smrt | 24. ožujka 1849. Jena, Tiringija, Njemačka |
| Državljanstvo | Nijemac |
| Polje | Kemija |
| Institucija | Sveučilište u Jeni |
| Poznat po | Periodni sustav elemenata Döbereinerove trijade |
| Portal o životopisima | |

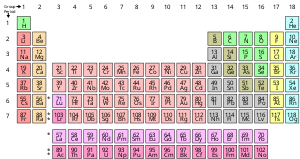
Izgradnja periodnog sustava elemenata
urediZa izgradnju kemijskih elemenata osnovno značenje pripada Paulijevu načelu, po kojemu pojedino stacionarno stanje u atomu može biti zaposjednuto samo od jednog elektrona. Prije nego što povučemo opće zaključke iz Paulijeva načela, predočit ćemo kako se postepeno izgrađuju kemijski elementi počevši od vodika. Od elemenata do elemenata pridolazi jedan elektron i morat ćemo uvijek razmisliti kuda da stavimo novi elektron.
Na početku periodnog sustava stoji vodik. U stabilnom stanju kreće se elektron u K ljuski i ima kvantne brojeve n = 1, l = m = 0 i s = 1/2.
Kuda da stavimo drugi helijev elektron? Naravno, u prazno energijsko najniže stanje. K ljuska sadrži još jedno stacionarno stanje, gdje spin ima antiparalelan položaj. Drugi elektron helija poprima, prema tome kvantne brojeve n = 1, l = m = 0 i s = - 1/2. Kako se vidi, oba helijeva elektrona kreću se u istoj stazi oko atomske jezgre, ali im vlastiti momenti impulsa stoje suprotno. Spini obaju elektrona poništavaju se među sobom, pa helijev atom ne smije imati ni impuls vrtnje ni magnetski moment. Pokusima je to potvrđeno.
Helijeva dva elektrona potpuno ispunjuju K ljusku. Litijev treći elektron prelazi u L ljusku. On ima kvantne brojeve n = 2, l = m = 0 i s = 1/2. Vanjski elektron litija kreće se daleko izvan K ljuske, pa tako litijev atom ima znatno veći promjer. Litij ima magnetski moment, koji potječe od spina vanjskog elektrona.
Kod idućeg elementa, berilija, dolazi još jedan elektron u L ljusku. Taj elektron razlikuje se od prvog s antiparalelnim položajem spina. Njegovi su kvantni brojevi n = 2, l = m = 0 i s = - 1/2. Vidi se da vanjska ljuska berilija nalikuje na helijevu elektronsku konfiguraciju. Time se objašnjava da berilij ima sličan s helijem, a nema kao ni helij magnetskog momenta.
L ljuska sadrži još kvantna stanja, gdje je impuls vrtnje l = 1. Kod petog elementa po redu, bora, treći elektron u vanjskoj ljuski poprima taj impuls vrtnje. Tri vanjska elektrona određuju valentnost bora, a treći vanjski elektron impuls vrtnje i magnetski moment.
Kod impulsa vrtnje l = 1 može magnetski kvantni broj m poprimiti vrijednost - 1, 0 i + 1. Pored toga može se spin postaviti paralelno i antiparalelno. Kako vidimo, imamo 6 različitih kvantnih stanja. Kvantni brojevi tih stanja jesu:
| glavni kvantni broj | orbitalni kvantni broj | magnetski orbitalni kvantni broj | magnetski spinski kvantni broj |
|---|---|---|---|
| n = 2 | l = 1 | m = + 1 | s = - 1/2 |
| n = 2 | l = 1 | m = 0 | s = - 1/2 |
| n = 2 | l = 1 | m = - 1 | s = - 1/2 |
| n = 2 | l = 1 | m = + 1 | s = + 1/2 |
| n = 2 | l = 1 | m = 0 | s = + 1/2 |
| n = 2 | l = 1 | m = - 1 | s = + 1/2 |
Ova kvantna stanja popunjuju redom elementi: bor, ugljik, dušik, kisik, fluor i neon. Posljednji element, neon, ima L ljusku dva elektrona s l = 0 i 6 elektrona s l = 1. Njegovi elektroni popunili su sasvim drugu ljusku. Vidimo opet da "plemeniti" potječe od popunjenosti vanjske ljuske. Osim toga, neon nema magnetskog momenta. Magnetski momenti njegovih 6 elektrona u svakom se smjeru poništavaju. Na elektron s m = + 1 dolazi elektron s m = - 1, a isto tako na s = + 1/2 dolazi s = - 1/2.
Neon ima 2 elektrona u K ljuski, a 8 u L ljuski. Kod jedanaestog po redu elementa, natrija, mora jedanaesti elektron prijeći u M ljusku. Vanjski elektron ima kvantne brojeve n = 3, l = m = 0 i s = + 1/2. Ovaj elektron, koji se podaleko kreće izvan popunjenih unutarnji ljusaka, prouzrokuje svojstva alkalijskih metala. Dvanaesti po redu element, magnezij, ima još jedan elektron u M ljuski. Staza tog drugog elektrona ista je kao i u prvog, samo što njegov spin stoji suprotno. Poput helija i berilija nema magnezij magnetskog momenta.
| Čvrsti | Broj stanja |
|---|---|
| s, m, l, n | 1 |
| m, l, n | 2 |
| l, n | 2∙(2∙l + 1) |
| n |
Suma u posljednjem redu tablice proračunata je jednostavno:
U ljuski s glavnim kvantnim brojem n ima mjesta za 2∙n2 elektrona. Taj rezultat je od osnovnog značenja za periodni sustav.
Stavljajući za glavni kvantni broj redom vrijednosti 1, 2, 3, 4, …, dobivamo najveći broj elektrona u različitim ljuskama. Popunjene ljuske sadrže elektrona:
| K | L | M | N |
|---|---|---|---|
| 2∙12 = 2 | 2∙22 = 8 | 2∙32 = 18 | 2∙42 = 32 |
K ljuska bila je ispunjena helijem, a L ljuska neonom. Ti elementi odista slijede u razmaku 2 i 8. Prva bi sad bila misao da se daljnja izgradnja elemenata vrši tako da se iduća M ljuska postepeno popuni elektronima. Vidjeli smo da to zaista tako ide do argona s rednim brojem 18. Međutim, dalje to ne ide više tako. Iako u M ljuski još ima mjesta za 10 elektrona, kod idućeg elementa, kalija, devetnaesti elektron prelazi u N ljusku. Razlog tome je što su energetski nivoi M ljuske s l = 2 viši od energetskih nivoa N ljuske s l = 0. U N ljuski staza l = 0 ulazi u unutarnje ljuske, kako smo vidjeli kod alkalijskih spektara, pa je elektron znatno čvršće vezan. U toj stazi mogu se kretati dva elektrona sa suprotnim smjerom spina. Takvu vanjsku konfiguraciju elektrona ima kalcij. On pripada metalima alkalijskih metala i ima dva elektrona u vanjskoj N ljuski. Idući element skandij s rednim brojem 21 stavlja svoj dvadeset i prvi elektron u M ljusku, koju su kalij i kalcij preskočili. Impulsu vrtnje l = 2 pripada 10 kvantnih stanja. Ta se kvantna stanja, počevši sa skandijem, postepeno popunjuju elektronima.
Zanimljivo je promatrati N ljusku. Kod nje kripton s rednim brojem 36 popunjuje dvije najniže podljuske l = 0 i l = 1. Trideset i sedmi elektron idućeg elementa, rubidija, preskače obje podljuske l = 2 i l = 3 u ljuski N i ide u O ljusku. Isto to čini i trideset i osmi element. Međutim, s trideset i devetim elementom počinje se opet popunjavati N ljuska i elektroni se smještaju u njenu podljusku l = 2. Kad se ta podljuska popuni, ne smještaju se novi elektroni u podljusku l = 3 ljuske N, nego prelaze u podljusku l = 1 ljuske O. Ta se podljuska popuni plemenitim plinom ksenonom. Sad opet nastupa jedan veliki skok, jer sljedeći element, cezij, stavlja svoj pedeset i peti elektron u P ljusku. Isto to čini i barij. Pedeset i sedmi element, lantan, stavlja svoj jedan elektron u O ljusku. Tek odsada počinje se postepeno ispunjavati slobodna, zadnja podljuska preskočene N ljuske. Ta podljuska s l = 3 sadrži 14 kvantnih stanja. No, toliko upravo ima rijetkih zemalja koje se nadovezuju na lantan. Sad razumijemo zašto su ti elementi tako kemijski srodni. Četrnaest elektrona ugrađuje se sukcesivno duboko u unutarnjim ljuskama. Atomska periferija ostaje pri tom u bitnom nepromijenjena. Zbog toga su slična sva svojstva rijetkih zemalja, koja ovise o periferiji atoma. Isto tako vidimo da ne može biti više od 14 rijetkih zemalja. Kod sedamdeset i drugog elementa, hafnija, prelazi već novi elektron u O ljusku.
Pri izgradnji periodnog sustava moramo imati dvoje pred očima. S jedne strane ljuske omataju jezgru onim redom kako idu slova abecede K, L, M, N, O, P i Q. No s druge strane, podljuske l = 0 i l = 1 viših ljusaka mogu imati nižu energiju nego podljuske l = 2 i l = 3 ili l = 4 prethodnih ljusaka. Zbog toga se izgradnja elemenata, kad idemo postepeno od vodika do uranija, ne vrši besprekidno na prvoj nepopunjenoj ljuski, nego se izvjesne podljuske preskoče, pa zatim grupe elemenata popunjuju preskočena kvantna stanja u unutarnjim ljuskama. Na osnovu toga možemo shvatiti sve zakonitosti u periodnom sustavu elemenata.[2]
Izvori
uredi- ↑ Döbereiner , Johann Wolfgang, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2019.
- ↑ Ivan Supek: "Nova fizika", Školska knjiga Zagreb, 1966.