Klorofil
Klorofil ili biljno zelenilo je zeleni biljni pigment, nužan u procesu fotosinteze, smješten u kloroplastima (plastidi), u svim zelenim dijelovima biljke. Klorofil imaju sve zelene biljke, alge i jedna skupina primitivnih fotosintetskih bakterija. U viših biljaka postoje dva kemijski srodna oblika klorofila, tamnije zeleni klorofil a i žutozeleni klorofil b. Međusobno se razlikuju po tome što klorofil a ima na drugom pirolskom prstenu metilnu skupinu (–CH3), a klorofil b na tome mjestu ima aldehidnu skupinu (–CHO). Kod algâ je utvrđeno nekoliko po građi srodnih klorofila, na primjer klorofil c kod smeđih alga i kremenjašica, a klorofil d kod crvenih algâ.[1] Klorofil se nalazi u kloroplastima te uz Sunčevu energiju, ugljikov dioksid i vodu stvara kisik i jednostavni šećer (glukozu). Kloroplasti su najviše zastupljeni u stanicama listova, što im daje prepoznatljivu zelenu boju. Klorofil a jedini sudjeluje u pretvorbi Sunčeve u kemijsku energiju. Ostali klorofili upijaju (apsorbiraju) svjetlost te prenose energiju na klorofil a.

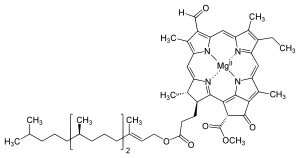


Struktura
urediStruktura molekule klorofila je porfirinski sustav građen od 4 pirolna prstena.U središtu molekule nalazi se atom magnezija. Molekula klorofila izgrađena je od četiriju pirolovih prstenova međusobno povezanih ugljikovim mostom koji čine tetrapirolski porfirinski prsten sličan onomu u hemu hemoglobina. U središtu porfirinskoga prstena klorofila nalazi se atom magnezija. Na prstenu se nalazi nekoliko različitih kemijskih skupina, na primjer vinilna, metilna ili aldehidna, etilna, izociklični pentanonski prsten, te propionska kiselina, na koju se esterski veže alkohol fitol, koji pridonosi dobroj topljivosti molekule u mastima i alkoholu.
Fotosinteza
urediSposobnost upijanja (apsorpcije) plavog i crvenoga dijela spektra Sunčeve svjetlosti klorofilu daju dvostruke povezane (konjugirane) kemijske veze između susjednih ugljikovih atoma u kojima se nalaze osobito gibljivi π elektroni. Oni ne pripadaju pojedinom atomu, već povezanom (konjugiranomu) sustavu kao cjelini. Za prijelaz u pobuđeno stanje (π → π*) takvu je elektronu dovoljan kvant ili foton vidljive svjetlosti. Posebna prstenasta struktura klorofila omogućuje da π elektroni osciliraju u prstenastom sustavu, a mogu i kružiti (cirkulirati). Klorofilne molekule mogu apsorbiranu svjetlosnu energiju prenositi na druge molekule i mogu je preuzeti od drugih molekula. Tako na primjer kod crvenih i smeđih algâ te cijanobakterija drugi pomoćni pigmenti – kao fikoeritrin, fukoksantin, fikocijanin – apsorbiranu energiju zelenoga dijela spektra predaju klorofilu a, najvažnijemu pigmentu fotosinteze.
Klorofili a i b u tilakoidnim membranama kloroplasta poredani su u takozvane fotosustave. Na rubu tih fotosustava nalaze se karotenoidi, koji dio primljene energije prenose na klorofile b i a, dio viška energije s pobuđenoga klorofila preuzmu i oslobode kao toplinu, a uz to zaštićuju klorofile od oksidativne fotodestrukcije koju uzrokuju prisutni superoksidni radikali.
Primjena
urediAlkoholni ekstrakt klorofila u prolaznom je svjetlu zelene boje, a u upadnome svjetlu fluorescira crveno. U alkoholnom ekstraktu listova obično se osim klorofila a i b nalaze i karotenoidi. Mućkanjem alkoholne otopine biljnog ekstrakta s benzenom mogu se odvojiti klorofili a, b i karoten od ksantofila. Daljnjom obradom s alkoholnom otopinom natrijeve lužine odvoji se alkohol fitol od klorofilidnoga dijela molekule, koji postane topljiv u alkoholnom sloju, a u benzenskom sloju zaostane žutonarančasti karoten. Klorofil se upotrebljava za bojenje ulja, masti, voskova te kao senzibilizator za fotografiju u boji.
Biljni pigmenti
urediPigment (lat. pigmentum: boja) je tvar različita kemijska sastava koja je nositelj boje u živih organizama. Nalaze se u stanicama u obliku zrnaca, kapljica i kristala; često su vezani na bjelančevine. Važni su za život biljaka, životinja i čovjeka. Podrijetlo im je dvojako: stvoreni su u protoplazmi specijalnih stanica kao endogeni pigmenti (plastidi) ili dospijevaju u stanice infiltracijom kao egzogeni pigmenti. Najrašireniji su pigmenti: porfirini (klorofil, hemoglobin, citokromi i drugi), karotenoidi (žuti ksantofili i narančasti do narančastocrveni karoteni, koji se nalaze u različitim tkivima biljaka, praživotinja, spužava, mahovnjaka, ježinaca, kralježnjaka, te fukoksantin u smeđih i nekih drugih alga), fikobilini (fikoeritrin i fikocijan), antocijani (crvene, ljubičaste i plave boje) te njihove bezbojne modifikacije leukoantocijanidini (bijela boja latica), flavoni i flavonoli (žute boje poznate i pod nazivom antoksantini; nalaze se u listovima, cvjetovima i plodovima biljaka, a dolaze i u nekih vrsta kukaca i ježinaca). U vakuolama većine biljaka reda Caryophyllales nalaze se crveni ili žuti betalaini, koji u svojoj molekuli sadrže dušik: betanidin u korijenu cikle, filokaktin u biljkama roda Phyllocactus, žuti pigment u zapadnoindijske opuncije. Takav je i amanitin, crveni pigment u otrovne gljive crvene muhare. U biljnom svijetu rašireni su i kinoni (primjerice smeđa jesenja boja listova kruške), a dolaze i u unutarnjim organima ježinaca i kukaca (naftokinoni). U perju, dlakama i koži životinja i čovjeka nalaze se melanini. Kod patoloških stanja pigmenti mogu biti abnormalno pojačani (na primjer kod žutice) ili ih nema (albinizam). Raspodjela pigmenata na površini (koži) ljudskoga, životinjskoga ili biljnoga organizma naziva se pigmentacija.
Klorofil kao pigment
urediKlorofil (C.I. 75810), smjesa je plavozelenog klorofila (a), C55H7205N4Mg, i žutozelenog klorofila (b), C55H7006N4Mg, najčešće u omjeru a:b = 2,5 ± 0,5. Klorofili a i b nalaze se vezani u kloroplastima zelenih dijelova svih biljaka s karotenoidima na lipoproteinskom nosaču. Neke biljke sadrže samo klorofil a ili samo klorofil b. Čisti klorofil a, u tankim, zelenim, šesterostranim pločicama, talište od 117 do 120 °C, može se dobiti kristalizacijom iz otopine u acetonu. Čisti klorofil b, u zelenim prizmama, talište od 120 do 130°C, može se dobiti kristalizacijom iz otopine u kloroformu i metanolu. U većim količinama klorofil se nalazi u lucerni ili plavoj djetelini (lat. Medicago sativa), u više vrsta kopriva (lat. Urtica dioica, U. urens), u divljem kupusu (lat. Brassica oleráceo) i mnogim drugim biljkama.
Klorofil otopljen u mastima i uljima upotrebljava se za bojenje sapuna, vegetabilnih, mineralnih i eteričnih ulja, voskova i farmaceutskih masti. U fotosintezi služi kao katalizator, a u fotografskom materijalu za apsorpciju infracrvenog zračenja. Služi i kao reagens za dokazivanje užeženosti ulja i masti. U vodi topljivi klorofilni preparati upotrebljavaju se u prehrambenoj industriji za bojenje kolača, želatine i pića, u kozmetičkoj industriji za bojenje paste za zube, a u farmaceutskoj industriji kao dodatak mastima ili otopinama za poticanje zarašćivanja ozljeda kože i za odstranjivanje neugodnog zadaha.[2]